人教版(2019)化学必修第一册《离子反应》PPT教学课件
展开
《离子反应》PPT教学课件
第一部分内容:素养目标
1.通过实验探究认识离子反应及其发生的条件,培养科学探究与创新意识。
2.会书写常见的离子方程式,并能进行正误判断,培养证据推理与模型认知能力。
3.复习酸、碱、盐的溶解性,结合电解质知识,掌握常见离子能否大量共存的判断方法,培养证据推理能力。
... ... ...
离子反应PPT,第二部分内容:课前篇自主预习
知识铺垫
1.复分解反应是指两种化合物互相交换成分,生成另外两种化合物的反应。其发生的条件为生成沉淀、放出气体或生成水。
2.写出a.H2SO4、b.NaOH、c.BaCl2在水溶液中的电离方程式:
(1)a和b两溶液混合后发生反应的化学方程式为H2SO4+2NaOH=Na2SO4+2H2O;
(2)a和c两溶液混合后发生反应的化学方程式为H2SO4+BaCl2=2HCl+BaSO4↓;
(3)b和c两溶液混合不能(填“能”或“不能”)发生复分解反应,原因是二者混合无气体、沉淀或水生成。
新知预习
一、离子反应
1.【实验1-3】
2.离子反应:电解质在溶液中的反应实质上是离子之间的反应,这样的反应属于离子反应。
3.离子反应的表示方法——离子方程式
(1)定义:用实际参加反应的离子符号来表示反应的式子。
(2)书写步骤(以Na2SO4溶液与BaCl2溶液的反应为例)
①写——写出化学方程式:Na2SO4+BaCl2=BaSO4↓+2NaCl。
②拆——把易溶于水且易电离的物质写成离子形式,难溶的物质、气体和水等仍用化学式表示:2Na++S +Ba2++2Cl-=BaSO4↓+2Na++2Cl-。
③删——删去方程式两边不参加反应的离子,并将方程式化为最简:S +Ba2+=BaSO4↓。
④查——检查离子方程式两边各元素的原子个数和电荷总数是否相等。
(3)意义
①[思考与讨论]
结论:强酸与强碱发生中和反应的实质是,强酸电离出的H+与强碱电离出的OH-结合生成H2O。
②离子方程式的意义
离子方程式不仅可以表示某个具体的化学反应,还可以表示同一类型的离子反应。
【微思考】离子方程式H++OH-=H2O只能表示强酸与强碱间发生的中和反应吗?
提示H++OH-=H2O还能表示某些盐与强碱间的复分解反应,如反应NaHSO4+NaOH=Na2SO4+H2O等。
二、离子反应的类型及发生反应的条件
1.类型:复分解反应和置换反应等。
2.复分解反应类型的离子反应发生的条件
自主测试
1.下列各组物质相互混合后,不会发生离子反应的是 ( )
A.Na2SO4溶液和MgCl2溶液
B.Na2CO3溶液和稀硫酸
C.NaOH溶液和Fe2(SO4)3溶液
D.Ca(OH)2溶液和盐酸
答案A
解析B项中C 和H+发生离子反应;C项中Fe3+和OH-发生离子反应;D项中OH-和H+发生离子反应。
2.下列离子方程式书写正确的是( )
A.盐酸与碳酸钡反应:
B.硫酸铜溶液中滴加氢氧化钠溶液:
2OH-+Cu2+=Cu(OH)2↓
C.SO3溶于水:
SO3+H2O=H2SO4
D.锌与稀盐酸反应:
Zn+H+=Zn2++H2↑
... ... ...
离子反应PPT,第三部分内容:课堂篇探究学习
离子方程式的书写与正误判断
问题探究
1.判断下列离子方程式的正误,并指出错误的原因。
(1)盐酸与Cu(OH)2反应:H++OH-=H2O( )
(2)CuO溶于盐酸:O2-+2H+=H2O( )
(3)Na2CO3溶液与稀硫酸反应:Na2CO3+2H+=2Na++CO2↑+H2O( )
(4)CuSO4溶液与Ba(OH)2溶液反应:Cu2++2OH-=Cu(OH)2↓( )
(5)CO2通入澄清石灰水变浑浊:CO2+Ca(OH)2=CaCO3↓+H2O( )
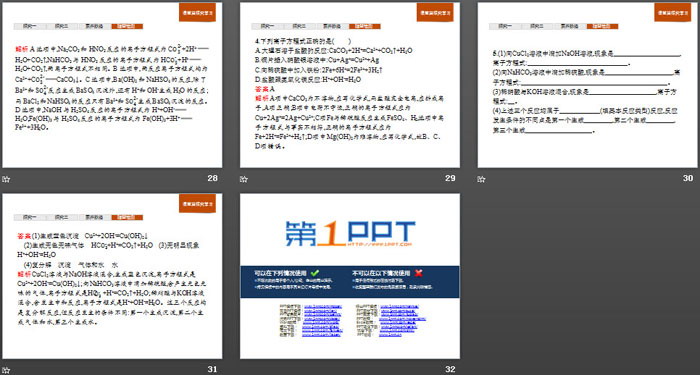
(6)NaHCO3溶液与稀硫酸反应:
CO_3^2"-" +2H+=CO2↑+H2O( )
(7)Fe与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑( )
(8)Cu与AgNO3溶液反应:Cu+Ag+=Ag+Cu2+( )
提示(1)错误,Cu(OH)2为难溶物,不能拆成Cu2+和2OH-。
(2)错误,CuO为氧化物,不可拆成Cu2+和O2-。
深化拓展
1.离子方程式的书写关键
书写离子方程式的关键是“拆”,且要“拆”得合理。
(1)熟记可“拆”的强酸、强碱和易溶盐。有关盐的溶解性口诀:钾钠铵盐都可溶,硝酸盐遇水无影踪,硫酸盐不溶硫酸钡,氯化物不溶氯化银。
(2)不能拆成离子的物质:难溶的物质、弱酸、弱碱、水(难电离的物质)、气体、单质、氧化物。
2.离子方程式正误判断的方法
(1)看离子反应是否符合客观事实。
不可主观臆造产物及反应,如2Fe+6H+=2Fe3++3H2↑就不符合客观事实。
(2)看表示各物质的化学式是否正确。
如多元弱酸的酸式酸根离子在离子方程式中不能拆开写,而
(3)看是否漏掉离子反应。
如Ba(OH)2溶液与CuSO4溶液反应,既要写Ba2+与S 的离子反应,又要写Cu2+与OH-的离子反应。
(4)看质量及电荷是否守恒。
如AgNO3溶液与Cu反应,不能写成Ag++Cu=Cu2++Ag,而应写成2Ag++Cu=Cu2++2Ag。
(5)看反应物或产物的配比是否正确。
归纳总结(1)可拆为离子的物质
①强酸:HCl、H2SO4、HNO3等。
②强碱:NaOH、KOH、Ca(OH)2、Ba(OH)2等。
③可溶性盐:NaCl、Na2SO4、NH4Cl等。
(2)不可拆为离子的物质
①单质:Cl2、Fe、Na等。
②氧化物:Na2O、CaO、CO2等。
③弱酸:H2CO3、CH3COOH、HClO、HF、H2S等。
④弱碱:NH3·H2O、Fe(OH)3、Cu(OH)2等。
⑤难溶物:AgCl、CaCO3、BaCO3等。
⑥水。
... ... ...
离子反应PPT,第四部分内容:随堂检测
1.下列各组物质间的反应中,不属于离子反应的是( )
A.Zn+H2SO4(稀) B.NaCl溶液+AgNO3溶液
C.C+O2 D.Fe+CuSO4溶液
答案C
解析A、B、D选项中的反应都是在溶液中进行的反应,且每一组中都有离子参与反应,所以都是离子反应;C与O2反应无论产物是CO还是CO2,都不是电解质在溶液中进行的反应,不属于离子反应。
2.下列各组离子能在溶液中大量共存的是( )
A.Na+、Mg2+、Cl-、OH- B.H+、Ca2+、CO_3^2"-" 、NO_3^"-"
C.Cu2+、K+、SO_4^2"-" 、NO_3^"-" D.Na+、HCO_3^"-" 、OH-、Ca2+
答案C
解析溶液中的离子能否大量共存,关键是看离子间能否发生反应。Mg2+和OH-能反应生成Mg(OH)2沉淀,即Mg2++2OH- Mg(OH)2 ↓; H+和CO_3^2"-" 、Ca2+和CO_3^2"-" 都能发生反应,即2H++CO_3^2"-" H2O+CO2↑,Ca2++ CO_3^2"-" CaCO3↓;HCO_3^"-" 和OH-、Ca2+和OH-都能反应,即HCO_3^"-" +OH- H2O+ CO_3^2"-" ,Ca2++2OH- Ca(OH)2↓;唯有选项C中的离子间不会发生反应。
3.下列同组中的两个不同反应(在溶液中进行),可用同一离子方程式表示的是( )
A.Na2CO3+HNO3与NaHCO3+HNO3
B.CaCl2+Na2CO3与Ca(NO3)2+K2CO3
C.Ba(OH)2+NaHSO4与BaCl2+NaHSO4
D.NaOH+H2SO4与Fe(OH)3+H2SO4
答案B
... ... ...
关键词:人教版高中化学必修一PPT课件免费下载,离子反应PPT下载,.PPT格式;