鲁科版(2019)化学必修第一册《氮的循环》物质的性质与转化PPT(第二课时氨的转化与生成)
展开
《氮的循环》物质的性质与转化PPT(第二课时氨的转化与生成)
第一部分内容:新课程标准是什么
1.了解氨的主要性质。
2.认识氨在生产中的应用和对生态环境的影响。
3.认识物质及其转化在自然资源综合利用和环境保护中的重要价值。
... ... ...
氮的循环PPT,第二部分内容:新知探究
氨的性质与应用
[自学新教材]
阅读教材,回答下列问题:
氨是氮循环中的重要物质,是氮肥工业和硝酸工业的重要原料,在人类的生产和生活中有着广泛的应用。
(1)完成下面实验。
(2)能否说NH3属于电解质?能否说NH3属于碱?
(3)工业上制备硝酸的流程如图,请结合图示写出工业上制备硝酸的化学方程式,并说明NH3在反应中表现的性质。
提示:(1)烧杯里的水由玻璃管进入烧瓶,形成喷泉,烧瓶内液体呈红色 NH3 +H2O��NH3•H2O、NH3•H2O��NH+4+OH-NH3为无色气体,极易溶于水,水溶液显弱碱性
集气瓶中产生大量白烟 NH3+HCl===NH4Cl NH3能够与酸反应生成盐
(2)NH3本身不能电离出NH+4、OH-,不属于电解质,也不属于碱。
(3)4NH3+5O2=====催化剂△4NO+6H2O(NH3表现还原性)、2NO+O2===2NO2、3NO2+H2O===2HNO3+NO。
[落实新知能]
1.NH3的性质和用途
(1)物理性质
(2)化学性质
NH3�D�D�D→H2ONH3+H2O��NH3•H2O�D�D�D→氯化氢NH3+HCl===NH4Cl;现象:产生白烟�D�D�D→催化氧化4NH3+5O2=====催化剂△14NO+6H2O,NH3 表现还原性
(3)氨的用途
①氨气易液化,用作制冷剂。
②用于合成硝酸、氮肥等。
2.氨水的性质
(1)成分:H2O、NH3、NH3•H2O、OH-、NH+4、H+。
(2)弱碱性:
①原因:NH3•H2O�鸠�NH+4+OH-。
②使红色石蕊试纸变蓝,使酚酞溶液变红。
(3)易分解(用方程式表示):
NH3•H2O�鸠�NH3↑+H2O。
[落实新知能]
1.判断正误(正确的打“√”,错误的打“×”)。
(1)氨水能导电,故NH3是电解质( )
(2)液氨和氨水是同一种物质( )
(3)氨气极易溶于水,所得溶液显碱性,其溶质是NH3•H2O( )
(4)用水做氨气的喷泉实验,可证明氨气的溶解度大小( )
(5)NH3中氮元素为-3,处于最低价态,具有一定的还原性,在一定条件下可被O2氧化( )
2.(2018•山东合格考)我国清代《本草纲目拾遗》中记载了药物“鼻冲水”,“贮以玻璃瓶,紧塞其口,勿使泄气,则药力不减,气甚辛烈,触人脑,非有病不可嗅”。“鼻冲水”指的是 ( )
A.酒精 B.氨水
C.烧碱 D.硫酸
3.氨水显弱碱性的主要原因是( )
A.通常状况下,氨的溶解度不大
B.氨水中的NH3•H2O电离出少量OH-
C.溶于水的氨分子只有少量电离
D.氨本身的碱性弱
4.能使湿润的红色石蕊试纸变蓝的气体是( )
A.Cl2 B.NH3
C.SO2 D.CO2
铵盐的性质与应用
[自学新教材]
阅读教材,回答下列问题:
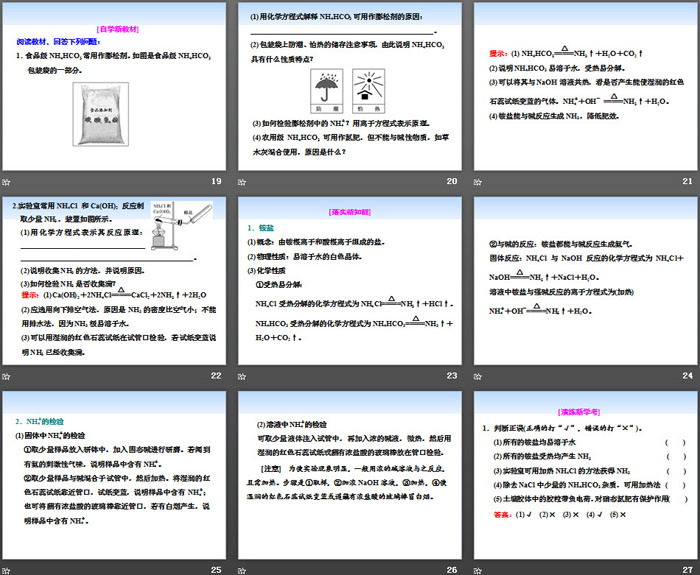
1.食品级NH4HCO3常用作膨松剂。如图是食品级NH4HCO3包装袋的一部分。
(1)用化学方程式解释NH4HCO3可用作膨松剂的原因:____________________________________________。
(2)包装袋上防潮、怕热的储存注意事项,由此说明NH4HCO3具有什么性质特点?
(3)如何检验膨松剂中的NH+4?用离子方程式表示原理。
(4)农用级NH4HCO3可用作氮肥,但不能与碱性物质,如草木灰混合使用,原因是什么?
2.实验室常用NH4Cl 和Ca(OH)2 反应制
取少量NH3,装置如图所示。
(1)用化学方程式表示其反应原理:__________________________________
_______________________________________________。
(2)说明收集NH3的方法,并说明原因。
(3)如何检验NH3是否收集满?
[落实新知能]
1.铵盐
(1)概念:由铵根离子和酸根离子组成的盐。
(2)物理性质:易溶于水的白色晶体。
(3)化学性质
①受热易分解:
NH4Cl受热分解的化学方程式为NH4Cl=====△NH3↑+HCl↑。
NH4HCO3受热分解的化学方程式为NH4HCO3=====△NH3↑+H2O+CO2↑。
2.NH+4的检验
(1)固体中NH+4的检验
①取少量样品放入研钵中,加入固态碱进行研磨。若闻到有氨的刺激性气味,说明样品中含有NH+4。
②取少量样品与碱混合于试管中,然后加热。将湿润的红色石蕊试纸靠近管口,试纸变蓝,说明样品中含有NH+4;也可将蘸有浓盐酸的玻璃棒靠近管口,若有白烟产生,说明样品中含有NH+4。
(2)溶液中NH+4的检验
可取少量液体注入试管中,再加入浓的碱液,微热,然后用湿润的红色石蕊试纸或蘸有浓盐酸的玻璃棒放在管口检验。
[注意]为使实验现象明显,一般用浓的碱溶液与之反应,且需加热。步骤是①取样,②加浓NaOH溶液,③加热,④使湿润的红色石蕊试纸变蓝或遇蘸有浓盐酸的玻璃棒冒白烟。
[演练新学考]
1.判断正误(正确的打“√”,错误的打“×”)。
(1)所有的铵盐均易溶于水( )
(2)所有的铵盐受热均产生NH3 ( )
(3)实验室可用加热NH4Cl的方法获得NH3 ( )
(4)除去NaCl中少量的NH4HCO3杂质,可用加热法 ( )
(5)土壤胶体中的胶粒带负电荷,对硝态氮肥有保护作用( )
2.以下性质不属于铵盐的通性的是( )
A.易溶于水 B.含有NH+4
C.可分解放出氮气 D.能与碱反应放出氨气
3.试管中盛有白色晶体,检验它是否是铵盐的方法中不可行 的是( )
A.加热,将湿润的红色石蕊试纸放在试管口
B.加氢氧化钠溶液,加热,将湿润的酚酞试纸放在试管口
C.加氢氧化钠溶液,加热,将蘸有浓盐酸的玻璃棒放在试管口
D.加氢氧化钠溶液,加热,将湿润的红色石蕊试纸放在试管口
喷泉实验及其原理
[难度增一点]
[典例] 喷泉是一种常见的自然现象,其产生的原因是存在压强差。
(1)制取氨气并完成喷泉实验(图中部分夹持装置已略去)。
①用图1装置进行喷泉实验,上部烧瓶已充满干燥氨气,引发水上喷的操作是______________________________。 该实验的原理是__________________________。
②如果只提供如图2的装置,请说明引发喷泉的方法:
__________________________________________________。
(2)利用图3装置,在锥形瓶中分别加入足量的下列物质,反应后可能产生喷泉的是________(填标号)。
A.Cu与稀盐酸
B.NaHCO3溶液与NaOH溶液
C.CaCO3与稀H2SO4
D.NH4HCO3与稀盐酸
(3)在图3锥形瓶中加入酒精,把锥形瓶放入水槽中,水槽中加入冷水后,再加入足量的下列物质,结果也产生了喷泉。水槽中加入的物质可以是________。
A.浓硫酸 B.食盐
C.硝酸钾 D.硫酸铜
(4)从产生喷泉的原理分析,图1、2是________上部烧瓶内的压强,图3是________下部锥形瓶内气体的压强(均填“增大”或“减小”)。人造喷泉及火山爆发的原理与上述装置图________原理相似。
[知能深一点]
喷泉实验及其原理
1.喷泉形成的原理
容器内外存在较大的压强差,在这种压强差的作用下,液体迅速流动,通过带有尖嘴的导管喷出来,即形成喷泉。
2.使容器内外产生较大的压强差的两类情况
(1)容器内气体极易溶于水或易与溶液中的溶质发生化学反应,从而使容器内气压迅速降低,如图A。
(2)容器内发生化学反应,产生气体。从而使容器内压强迅速增大,促使容器内液体迅速向外流动,形成喷泉。例如,喷雾器、人造喷泉等均是利用了此原理,如图B。
A.通过挤压胶头滴管,使氨气溶于水造成烧瓶内压强变小。
B.CaCO3与HCl反应,生成CO2气体,使锥形瓶内压强变大。
3.做好氨的喷泉实验的关键
(1)装置的气密性要好,检验的方法是连接装置后,打开止水夹,将玻璃管下端浸入水中,双手捂紧圆底烧瓶,若玻璃管内有气泡冒出,且松开手后玻璃管内液体回流形成一段稳定液柱,则说明该装置的气密性良好。
(2)圆底烧瓶必须保持干燥。
(3)圆底烧瓶要尽可能集满气体,若气体量不足,则难以形成喷泉。
(4)烧杯内必须装入足量的水,以防止因水的量不足而造成喷泉现象停止或不发生。
... ... ...
关键词:鲁科版高中化学必修一PPT课件免费下载,氮的循环PPT下载,物质的性质与转化PPT下载,氨的转化与生成PPT下载,.PPT格式;