人教版(2019)化学必修第一册《氧化剂和还原剂》氧化还原反应PPT
展开
《氧化剂和还原剂》氧化还原反应PPT
第一部分内容:目标与素养:
1. 认识氧化剂、还原剂、氧化性、还原性等基本概念。(宏观辨识与微观探析)
2.了解常见的氧化剂、还原剂。(宏观辨识)3.了解氧化还原反应的应用。(科学态度与社会责任)
... ... ...
氧化剂和还原剂PPT,第二部分内容:自主预习探新知
一、氧化剂和还原剂
1.概念
(1)氧化剂:在反应中_______________ 的物质。
(2)还原剂:在反应中_______________ 的物质。
2.联系
3.常见氧化剂和还原剂
微点拨:理解氧化还原反应的相关概念,要抓住两条线:
①还原剂化合价升高→失去电子→发生氧化反应(被氧化)→生成氧化产物。
②氧化剂化合价降低→得到电子→发生还原反应(被还原)→生成还原产物。
二、氧化性和还原性
1.氧化性和还原性
(1)氧化性:表示氧化剂_______能力强弱的性质。
(2)还原性:表示还原剂_______强弱的性质。
2.氧化性、还原性和元素化合价之间的关系
三、生产生活中的氧化还原反应
1.积极作用:金属冶炼、电镀、燃料燃烧、绿色植物的光合作用等。
2.负面影响:易燃物的自燃、食物的腐坏、钢铁的锈蚀等。
... ... ...
氧化剂和还原剂PPT,第三部分内容:核心突破攻重难
物质氧化性、还原性强弱的比较
1.根据氧化还原反应方程式比较
氧化剂+还原剂�D→还原被还原产物+氧化被氧化产物
氧化性:氧化剂>氧化产物;还原性:还原剂>还原产物。
2.根据金属的活动性顺序判断
3.根据氧化还原反应的程度比较
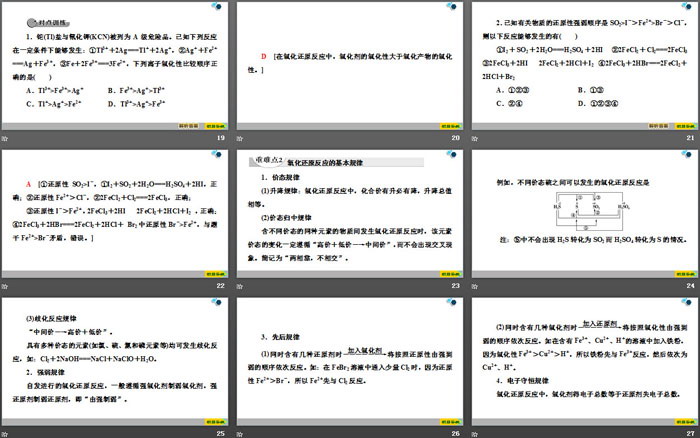
不同氧化剂与相同还原剂作用时,还原剂化合价升高的数值越大,氧化剂的氧化性越强。
4.根据反应的条件及反应的剧烈程度比较
反应条件要求越低,反应越剧烈,对应物质的氧化性或还原性越强,如是否加热、反应温度高低、有无催化剂和反应物浓度大小等。
... ... ...
氧化剂和还原剂PPT,第四部分内容:当堂达标提素养
1.氢化钙可以作为生氢剂(其中CaH2中氢元素为-1价),反应方程式如下:CaH2+2H2O===Ca(OH)2+2H2↑,其中H2是( )
A.既是氧化产物又是还原产物
B.是氧化剂
C.是还原剂
D.既是氧化剂又是还原剂
A [反应中CaH2中氢元素由-1价升高至0价,H2O中氢元素由+1价降低至0价,氢气既是氧化产物又是还原产物。]
2.在下列反应中,二氧化碳作氧化剂的是( )
A.Ca(OH)2+CO2===CaCO3↓+H2O
B.CO2+C=====高温2CO
C.2Fe2O3+3C=====高温4Fe+3CO2↑
D.CuO+CO=====△Cu+CO2
B [选项A中二氧化碳中碳元素化合价无变化;选项B中二氧化碳中碳元素化合价由+4价降低为+2价,作为氧化剂;选项C、D中二氧化碳都为氧化产物。]
... ... ...
关键词:人教版高中化学必修一PPT课件免费下载,氧化剂和还原剂PPT下载,氧化还原反应PPT下载,.PPT格式;